
Evolution de l’endomètre dès lors qu’il y a eu fécondation
Le blastocyste (embryon) et l’endomètre doivent communiquer (par l’intermédiaire de récepteurs et de signaux) et se modifier en même temps afin que le blastocyste puisse s’implanter.
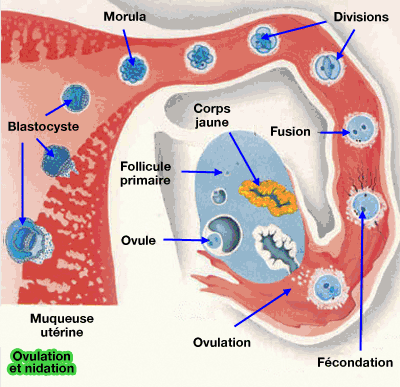
L’implantation du blastocyste demande plusieurs étapes :
-
L’orientation du blastocyste
-
L’apposition du blastocyste
-
L’adhésion du blastocyste à l’épithélium utérin
-
L’invasion aboutissant à l’enfouissement complet de l’oeuf dans le stroma utérin avec reconstitution de l’épithélium de surface

1- L'orientation

Le blastocyste s’oriente de sorte que son pôle embryonnaire soit face à l’endomètre.
Au stade du blastocyste, les cellules du trophoblaste commencent à absorber les nutriments fournis par les glandes épithéliales de l’utérus. Cela provoque la croissance de l'embryon et exerce une pression sur la zone pellucide. Cela conduit à sa rupture et à l'éclosion de l'embryon
Le blastocyste va donc éclore :

2- L’apposition
Lorsque l’embryon a quitté la zone pellucide, les trophoblastes peuvent interagir avec l’épithélium de l’endomètre. Sous l'influence de médiateurs solubles, libérés par les trophoblastes et les cellules épithéliales, des modifications se produisent dans les deux types de cellules qui permettront à terme leur adhésion (suivie de l'implantation du blastocyste). :
-
Apparition de pinopodes : petites protubérances de l’endomètre ressemblant à des doigts, leur développement est stimulé par la progestérone mais inhibé par les œstrogènes .
-
Raccourcissement voir perte des microvillosités ( cils contenant de la tubuline qui font des mouvements et permettent le mouvement des spermatozoïdes)
Les pinopodes absorbent une partie du liquide utérin via endocytose, diminuant ainsi le volume de la cavité utérine; ce qui engendre un effet d'aspiration qui va rapprocher la blastocyste de la paroi de l'endomètre.

pinopodes
3- L'adhésion
L'identité des molécules sur le trophoblaste et les épithéliums de l'endomètre qui assurent l’adhésion entre les deux restent non identifiées. Cependant, un certain nombre de groupes de recherche ont proposé que la Mucine-1 (MUC-1), une molécule de la famille des mucines, des protéines glycosylées, serait impliquée. La MUC-1 est une glycoprotéine transmembranaire exprimée à la surface des cellules épithéliales de l'endomètre au cours de l'implantation du blastocyste. La MUC1 affiche des fractions glucidiques sur son domaine extracellulaire qui sont des ligands de la L-sélectine, une protéine exprimée à la surface des cellules du trophoblaste. L'hypothèse selon laquelle la L-sélectine induirait l'apposition du blastocyste sur l'épithélium utérin en interagissant avec ses ligands serait la plus probable.

MUC-1

Le blastocyste va se fixer à l'épithélium utérin grâce à la sécrétion de facteurs qui se lient à des récepteurs spécifiques (un tissu synthétise le ligand, l'autre exprimer le récepteur).
De nombreuses molécules interviennent dans ce processus complexe :
-
Leukemia Inhibiting Factor (LIF) : les effets du LIF se font sentir à la fois sur l'endomètre et sur le blastocyste, ils conduisent à l'expression de gènes qui aident les trophoblastes à pénétrer dans l'endomètre. Le LIF améliore également l'expression de MUC1, à laquelle le blastocyste peut se lier avec sa molécule d'adhésion L-sélectine.
-
L’interleukine 1 (IL 1): cytokine inflammatoire, son rôle dans le fonctionnement des trophoblastes reste flou. Il pourrait jouer un rôle dans l'adhérence entre la MUC1 et la L-sélectine, mais jusqu'à présent, il est difficile de déterminer lesquelles sont essentielles à l'implantation du blastocyste.
-
Epidermal Growth Factor (EGF-R) : facteur de croissance épithélial (EGF) et son récepteur EGF-R, exprimé par les cellules du trophoblastes qui favorise leur prolifération.
-
Human chorionic gonadotropin (hCG) :
La gonadotrophine chorionique humaine est une hormone qui permet le maintien du corps jaune pendant le début de la grossesse, ce qui lui permet de sécréter de la progestérone. Cette hormone est libérée par les trophoblastes et permet au blastocyste de s'implanter correctement dans l'endomètre. Elle permet aussi une production locale accrue de lymphocytes T cytotoxiques qui inhibent la réponse immunitaire adaptative. Cela est important car l’embryon contient des «protéines non autonomes» qui peuvent entraîner une réaction de rejet (comme cela se produirait avec des organes greffés provenant d’un donneur non compatible).
4- L'invasion
L'invasion est le processus qui conduit à l'enfouissement complet de l'embryon dans l’endomètre ou le stroma utérin.
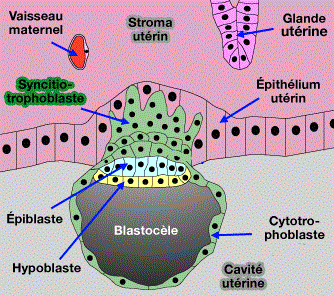
Au moment de l'implantation, le trophoblaste qui est en contact avec l'endomètre, se différencie en deux couches à partir du 7ème jour du développement :
-
Le cytotrophoblaste est le tissu épithélial interne qui encercle l'embryoblaste (épiblaste + hypoblaste) et le blastocèle.
-
Le syncytiotrophoblaste qui prolifère pour former un syncytium (cytoplasme à plusieurs noyaux).

L’implantation du blastocyste dans l’endomètre se fait grâce au syncytiotrophoblaste. Il absorbe grâce à des enzymes protéolytiques les cellules de l’endomètre et ses capillaires. Son développement rapide permet d’entourer entièrement le blastocyste.


Le syncytiotrophoblaste produit des travées cellulaires appelées invadopodes.
Ils ont pour rôle d’écarter les cellules épithéliales et de se lier à la laminine de la membrane basale par des intégrines. Ils digèrent la membrane basale et les cellules de l'endomètre ainsi que ses capillaires grâce à des métalloprotéinases (enzymes capables de détruire toutes sortes de protéines de la matrice extracellulaire) et des activateurs du plasminogène (protéines impliquées dans la dégradation des caillots sanguins).
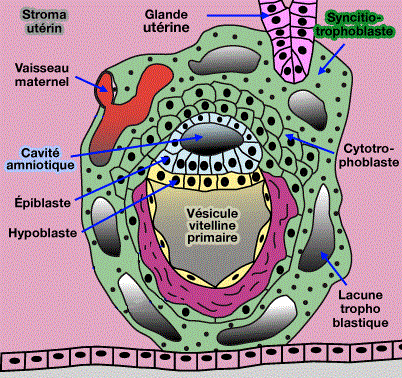
Le syncytiotrophoblaste digère les cellules utérines et synthétise des lacunes trophoblastiques qui se remplissent d’un liquide nutritif, appelé embryotrophe composé de sang maternel issu des capillaires rompus et de sécrétions des glandes altérées de l'endomètre.
La croissance du syncytiotrophoblaste est ensuite bloquée par des inhibiteurs protéiques synthétisés par les cellules déciduales pour éviter un développement trop important.
Ces cellules déciduales sont à l’origine des cellules issues du tissu conjonctif de l’endomètre qui ont subi une transformation, on appelle ce phénomène la réaction déciduale. Les cellules déciduales mortes sont digérées par le syncytiotrophoblaste et serviront de nutriments au blastocyste avant la création de la circulation foeto-placentaire.

